近日,省重点实验室范衠教授及其硕士研究生韦家弘、莫嘉杰和博士研究生朱贵杰与南开大学刘进超副教授、汕头大学容毅标博士、李文姬博士和苏州大学陈新建教授共同完成的论文《Genetic U-Net: automatically designed deep networks for retinal vessel segmentation using a genetic algorithm》被SCI医学成像顶刊《IEEE Transactions on Medical Imaging》(影响因子:10.048分,医学-成像科学与照相技术1区,2/51;医学-计算机科学应用1区,21 / 693)录用。
在临床中,医生们通过眼底图像观察视网膜血管系统以诊断眼科疾病或者其他全身性疾病,如青光眼,年龄相关性黄斑变性疾病和糖尿病等。这些疾病会导致视网膜血管形态的改变,对视网膜血管进行精确分割获得血管的形态信息可以辅助医生诊断或跟踪这些疾病。然而,医生们手动分割视网膜血管具有强主观性、耗时和繁琐等缺点。近年来,为了提高诊断效率,基于深度神经网络模型的自动视网膜血管分割算法因其良好的分割效果成为了主流(特别是基于U-Net的算法)。然而,现有用于视网膜血管分割的神经网络模型在临床应用中仍然存在以下两个不足: 1)对视网膜血管的特征提取能力不足;2)模型的参数量较大,因此模型计算复杂度高和容易过拟合。我们通过观察发现这些模型都是通过重复堆叠相同结构的模块构建整个网络,但使用相同结构的模块来处理不同模式的眼底图像特征是不合理的,这也是造成以上两个不足的主要原因。同时,手工设计出具有不同结构模块和较少参数的高性能网络模型有着较高的专业知识要求和较大的工作量。基于此,该工作提出了一种新颖的进化神经架构搜索方法,基于特定的搜索空间和改进的遗传算法自动搜索出性能更佳的U型深度神经网络架构(Genetic U-Net),该方法总体框架如图1所示。
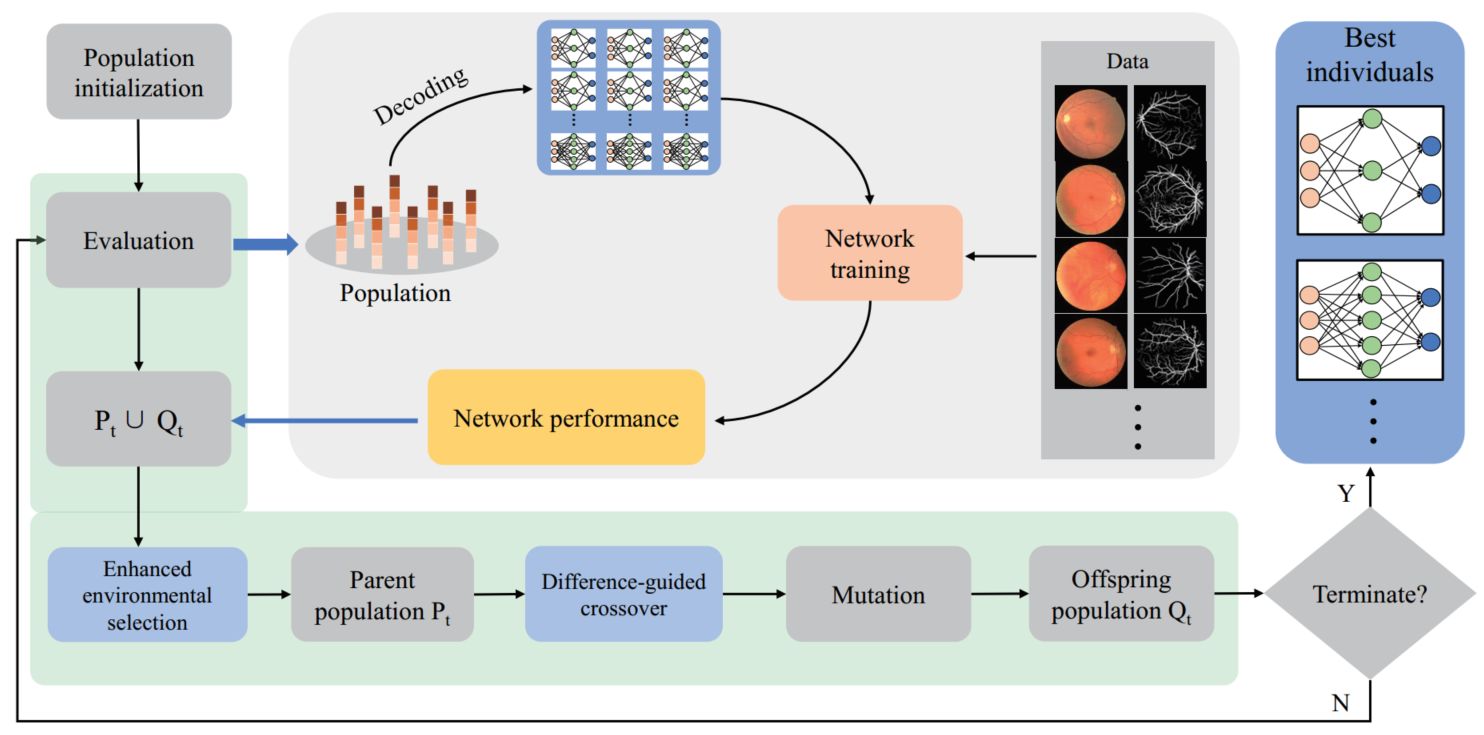
图1 Genetic U-Net总体流程框架
具体地,考虑到U型编解码器在图像分割任务上的通用性和神经架构搜索的计算效率,该方法首先设计了一个基于U型编解码器的紧凑但灵活的搜索空间,使U型编码器和解码器的每个模块都能单独且灵活地进行结构和相应超参数优化,克服了手工设计方法通常只能设计单一模块的局限。然后,为了减少神经架构搜索过程的计算消耗和促进该方法得到一个参数效率较高的高性能网络架构,我们使用改进的遗传算法在该搜索空间中优化迭代挖掘出高性能的网络结构,并探索了在更少结构参数下找到更优网络结构的可能性。
在实验结果方面,与其他SOTA算法相比,该方法得到的模型以仅仅0.27 M的结构参数(少于原始U-Net的1%)在四个常用的视网膜血管分割公开数据集DRIVE、STARE、CHASE_DB1和HRF上,均以最少的结构参数获得了最好的分割效果。特别地,该方法得到的模型对眼底图像中挑战性区域(如低对比度的微小血管、光照不均衡区域和病变区域等)的分割效果也明显优于其他SOTA网络模型(U-Net、FC-DenseNet、CE-Net、CS2-Net等),上述分割效果如图2和图3所示。此外,Genetic U-Net在DRIVE数据集上搜索到的模型也在细胞边界分割任务进行了测试(如图4所示),结果表明该方法得到的模型性能同样优于上述SOTA网络模型,也体现出Genetic U-Net在其他医学图像分割任务上的较强泛化能力。

图2 不同模型在四种公开数据集上的分割结果

图3 不同模型在眼底血管不同区域的分割结果 图4 不同模型在细胞边界分割任务上的结果
在这项工作中,我们还通过对进化结果中最后一代的网络结构进行观察和统计分析,提取出一些能提高视网膜血管分割效果的神经网络结构设计的知识和准则。这些知识和准则将有助于未来神经网络架构的设计,也有助于推动相关神经网络算法的临床应用落地。
论文下载:【Download PDF】
代码链接:https://github.com/96jhwei/Genetic-U-Net
论文引用:
J. Wei, G. Zhu, Z. Fan*, J. Liu, Y. Rong, J. Mo, W. Li, X. Chen*. Genetic U-Net: automatically designed deep networks for retinal vessel segmentation using a genetic algorithm[J]. IEEE Transactions on Medical Imaging, DOI: 10.1109/TMI.2021.3111679. ( JCR: Q1, IF:10.048 )
|
